土耳其医疗器械监管机构为土耳其药品和医疗器械管理局TITCK(Türkiye İlaç ve Tıbbi Cihazlar Kurumu)。TITCK的主要职责为:医疗器械的市场准入审查、法规制定与执行、市场监测与后续审查。
Tibbi Cihaz Yönetmeliği, Official Gazette No. 31499【医疗器械法规,第31499号官方公报】
按土耳其医疗器械法规要求,土耳其医疗器械注册也需要遵守欧盟MDR 2017/745(《医疗器械法规》)和IVDR 2017/746(《体外诊断医疗器械法规》)
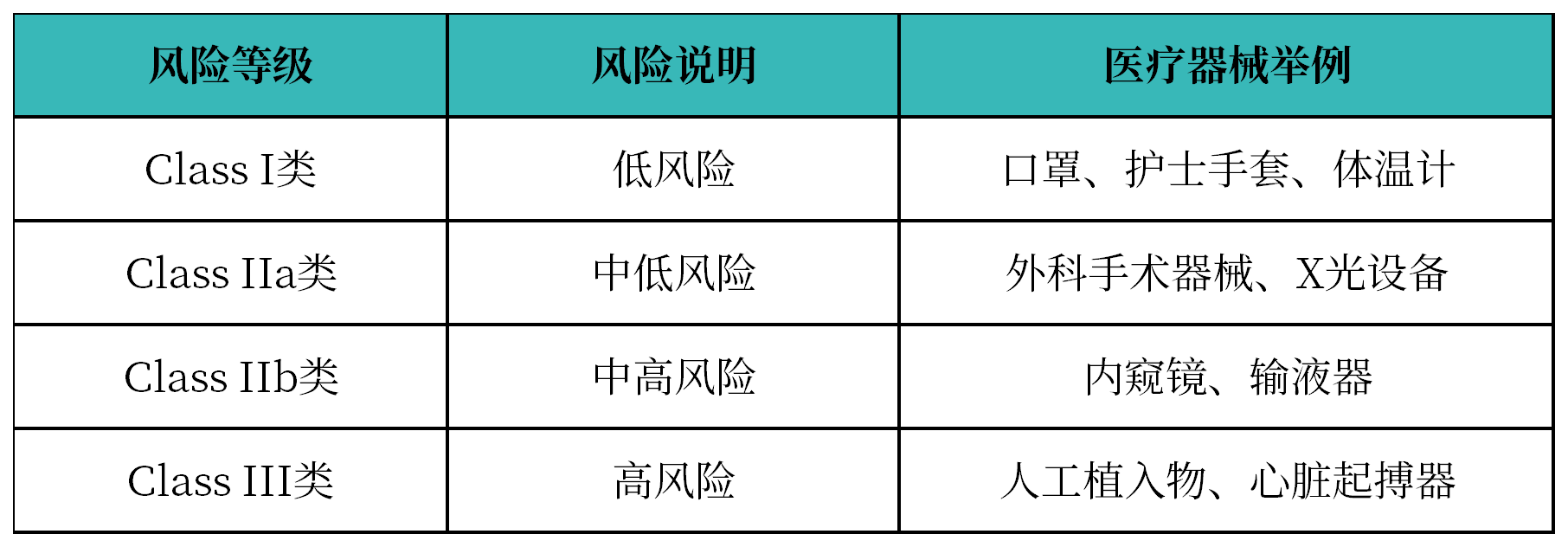
土耳其医疗监管机构将医疗器械分为:Class I类、Class IIa类、Class IIb类和Class III类:
土耳其医疗监管机构将IVD分为:Class A类、Class B类、Class C类和Class D类:

土耳其医疗器械注册监管要求进口产品必须已通过CE注册或认证,加贴 CE 标志,并在EUDAMED数据库中进行医疗器械注册。
土耳其语
根据土耳其的相关法规,土耳其医疗器械持证人是指在土耳其境内负责医疗器械注册申请,并持有土耳其医疗器械注册证书的法人或实体。
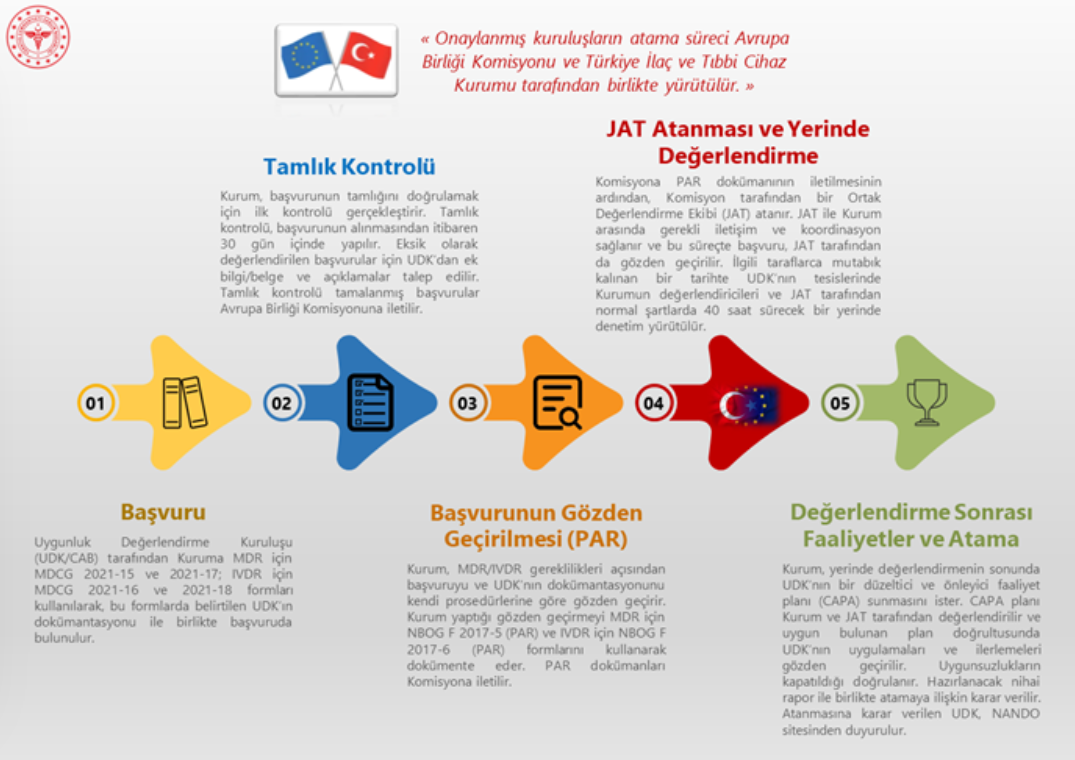
1.注册流程
2.注册周期及官费
土耳其医疗器械/IVD注册周期为:1-6个月
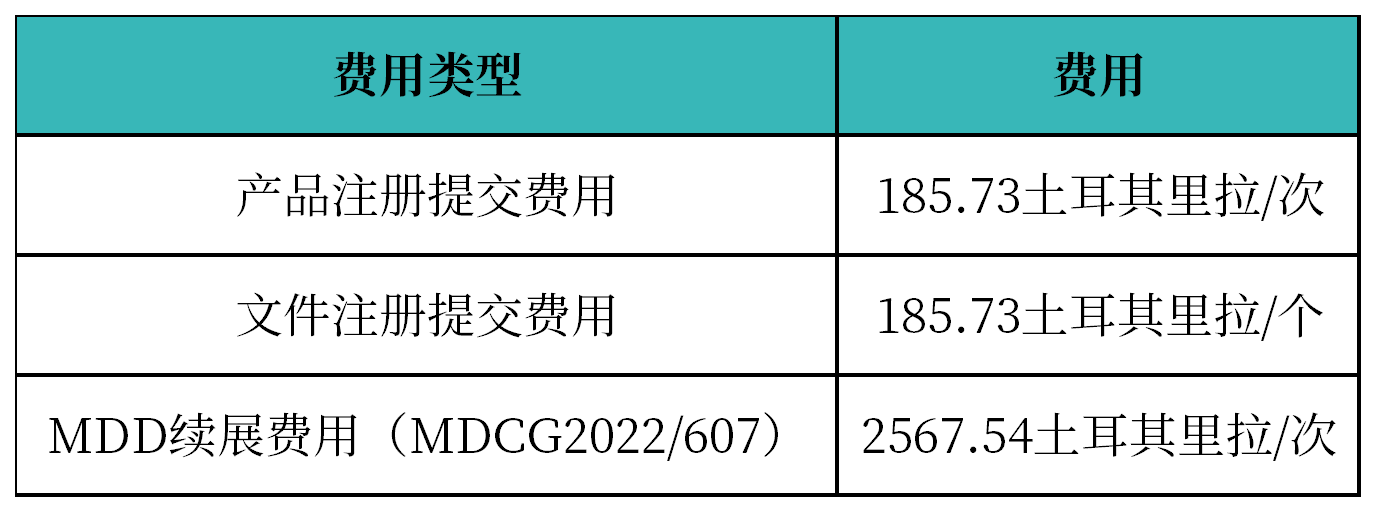
官费: