


尼日利亚医疗器械由国家食品药品监督管理局(National Agency for Food and Drug Administration and Control,简称NAFDAC)统一监管,是WHO认证的Maturity Level 3(ML3)国家级监管机构,核心职责包括:医疗器械法规制定、市场准入审批、生产与进口环节监督、上市后质量监测及执法管理。
NAFDAC Act CAP N1 (LFN) 2004
尼日利亚医疗器械按风险等级分为Class A、Class B、Class C和Class D四类,风险等级依次升高:
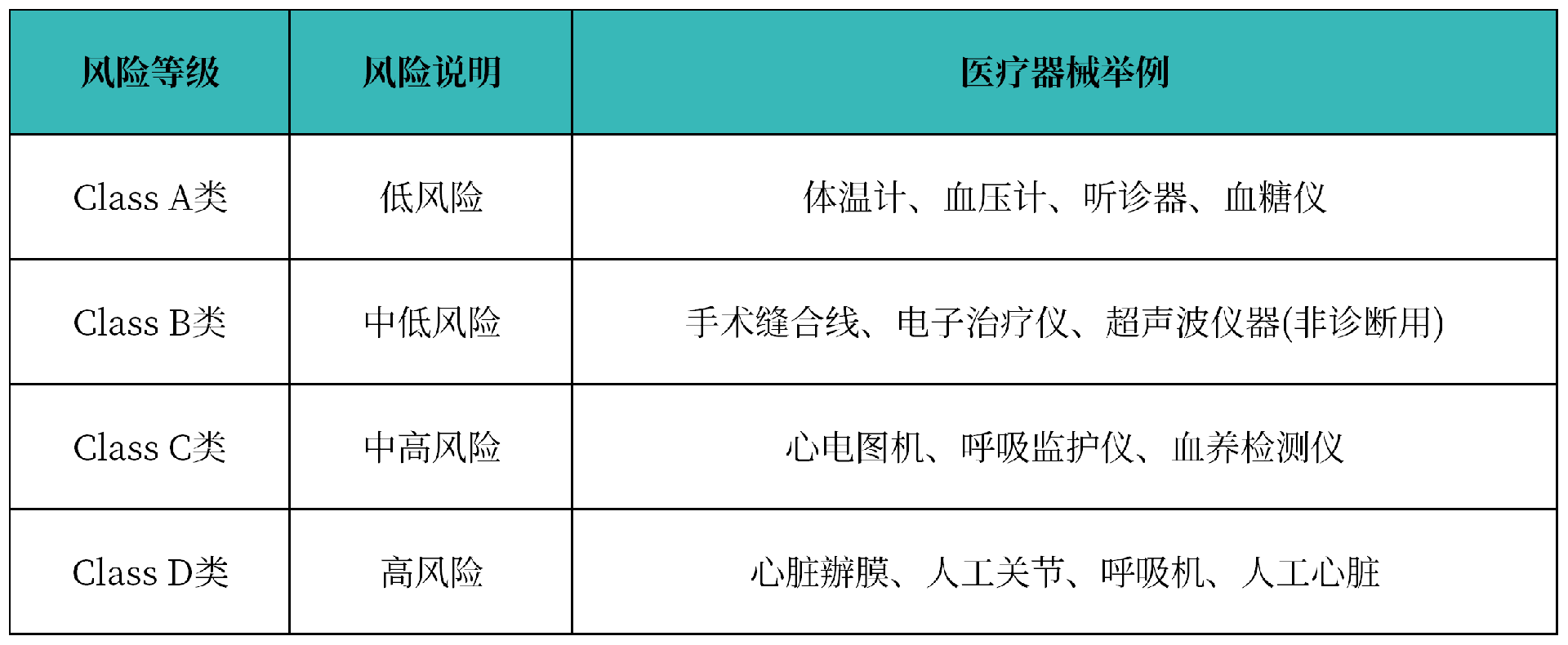
体外诊断试剂(IVD)产品同样按风险等级分为Class A、Class B、Class C和Class D四类:
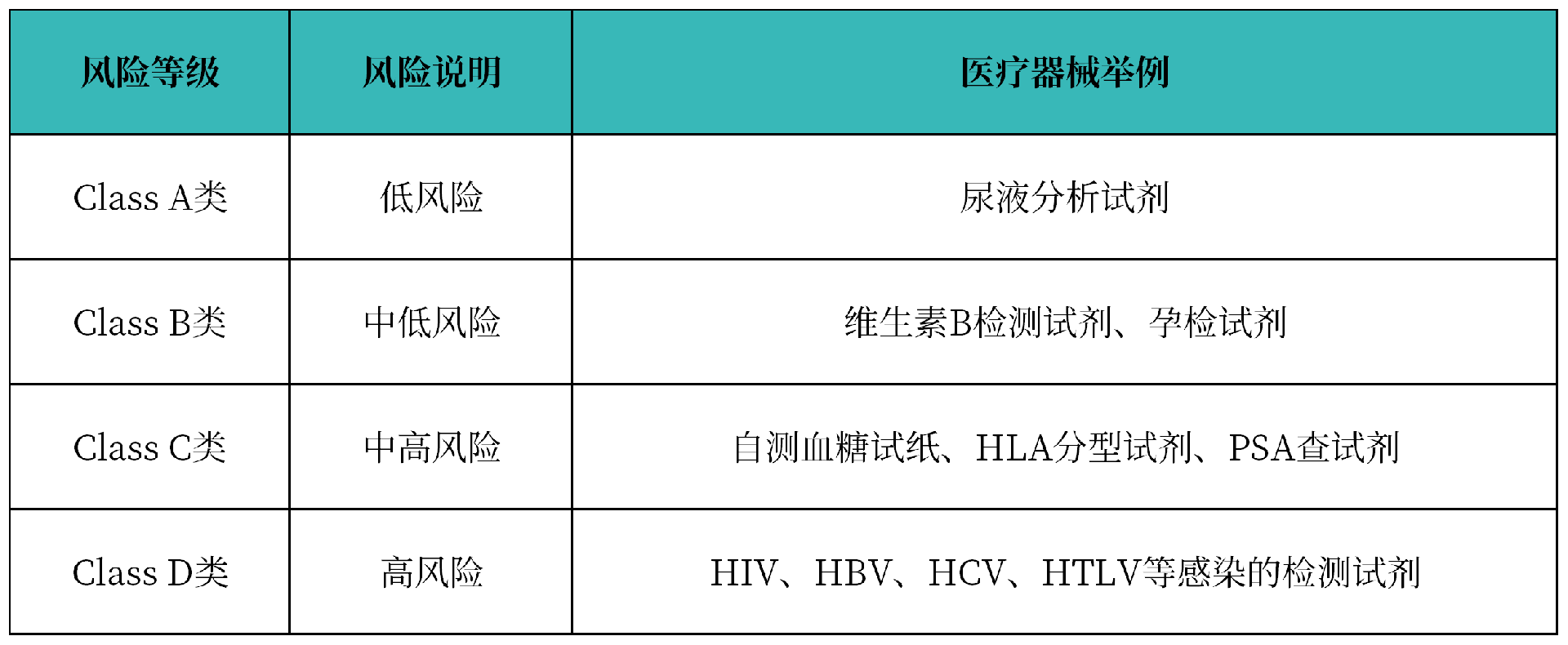
英语
NAFDAC强制要求境外制造商必须委任一位尼日利亚本地合法注册且获得NAFDAC认可的代理人,由其负责提交注册申请及后续沟通事宜。
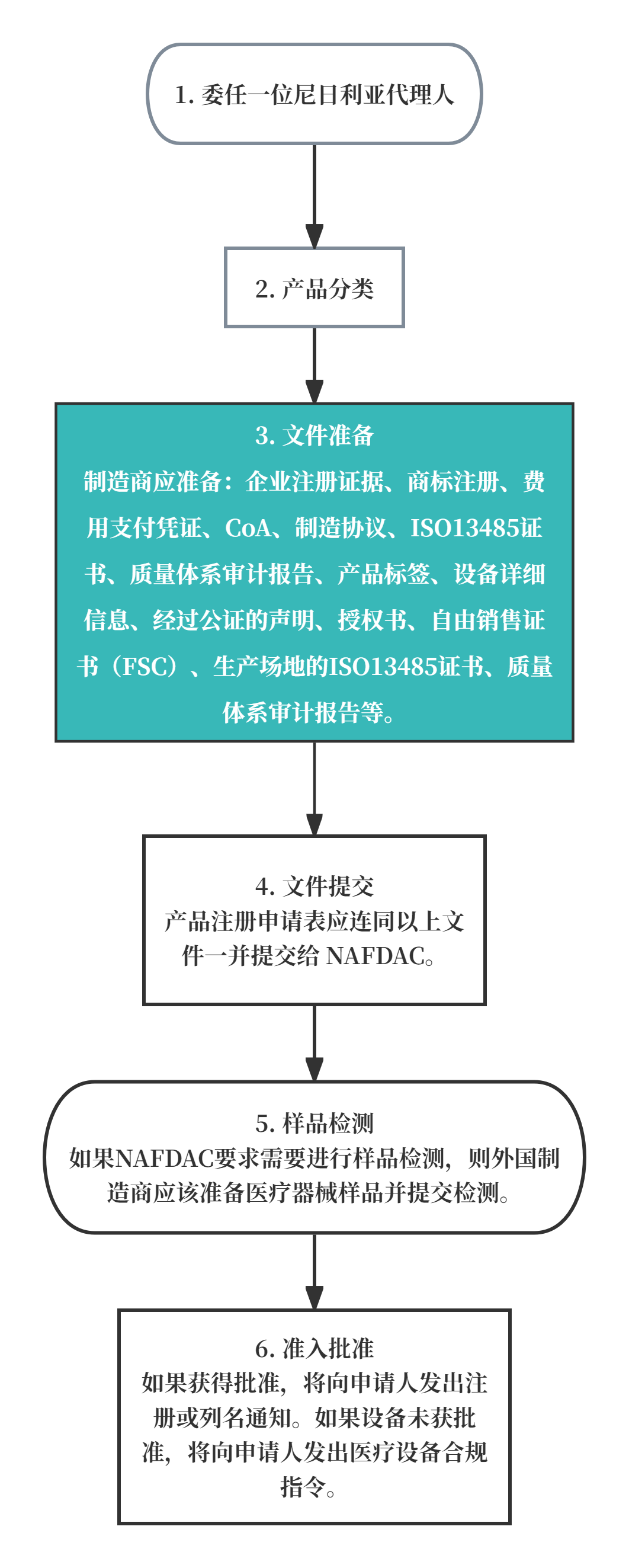
标准流程:委任尼日利亚本地注册代理人→确定产品风险等级分类→准备完整注册文件(企业资质、ISO 13485证书、自由销售证书、产品技术资料等)→通过代理人向NAFDAC提交注册申请→NAFDAC开展文件审核→根据要求提交产品样品进行检测→审核通过,颁发注册/列名通知;审核不通过,发出医疗设备合规指令。
资料完整且合规的情况下,NAFDAC常规审核周期约为8个月。
统一官费:874美元/个产品