


埃及药品监督管理局(Egyptian Drug Authority,简称 EDA)是卫生部的下属机构,负责通过监管药品(人类和兽医)、生物制剂、医疗器械、化妆品、膳食补充剂和杀虫剂的安全和质量来保障人民健康。
Law No. (151) of 2019.
Egyptian Medical Device Law Law No. 10 of 2003
医疗器械分类:埃及将医疗器械分为四类,从低风险到高风险分别为 Class Ⅰ 类、Class Ⅱa 类、Class Ⅱb 类和 Class Ⅲ 类。

IVD 产品分类:


①ISO 13485 质量管理体系
②若在埃及无当地实体,必须指定一名埃及注册持有人(Egypt Registration Holder,简称 ERH)
③所有医疗器械都必须在埃及药品管理局(EMA)注册。申请注册许可需提供完整的技术文件
④符合性声明
⑤ISO 证书
⑥FSC
⑦授权书
家用仪器使用标签必须以阿拉伯语提供,专业使用仪器标签必须以阿拉伯语或英语提供。
在埃及医疗器械注册过程中,ERH(埃及当地授权代表)是指制造商在埃及指定的当地代表,帮助制造商在埃及进口设备并负责该地区的上市后监督活动。ERH的职责包括在埃及进口设备、处理与埃及药品管理局(EDA)的沟通、处理上市后监督等。
ERH的作用和重要性:
沟通桥梁:ERH是制造商与埃及当地监管机构之间的桥梁,负责处理与EDA的沟通和协调工作。
上市后监督:ERH负责在埃及的上市后监督活动,确保医疗器械在市场上的合规性和安全性。
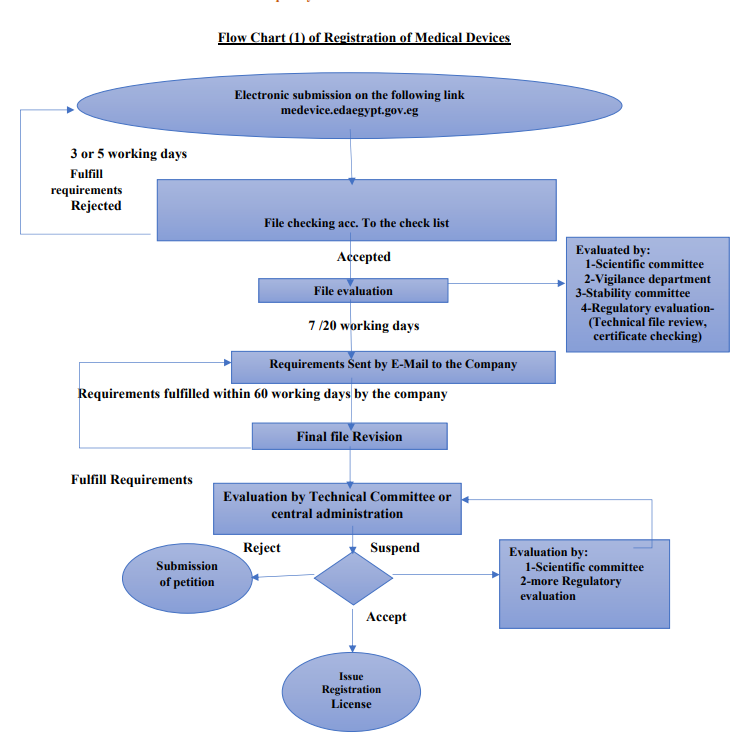
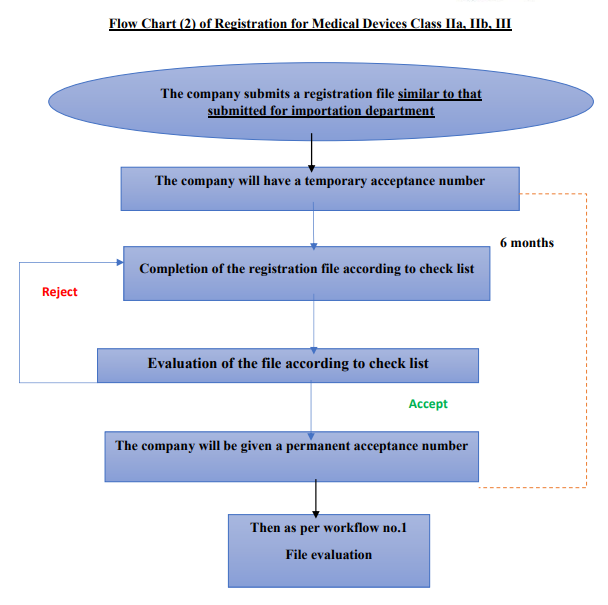

注册周期:
根据Wiselink项目经验以及相关法规概述,审查技术文件可能需要长达 30 个工作日,制造商有 60 个工作日的时间来回应 EDA/DPPC 提出的意见。DPPC 在完成验证后会颁发进口批准,而 EDA 会颁发营销授权,其验证活动可能需要长达 18 个月。
官方费用:
进口医疗器械注册文件的评估/审查:普通通道:98 美元,快速通道注册:421 美元