

埃塞俄比亚医疗器械监管部门

埃塞俄比亚医疗器械注册的监管机构为埃塞俄比亚食品、药品和医疗器械管理局Ethiopian Food and Drug Authority(EFDA),隶属于卫生部。
EFDA主要负责医疗器械的市场准入、质量管理、上市后监管等。
Food and Medicine Administration Proclamation 1112
GUIDELINE FOR REGISTRATION OF MEDICAL DEVICES
医疗器械分类:
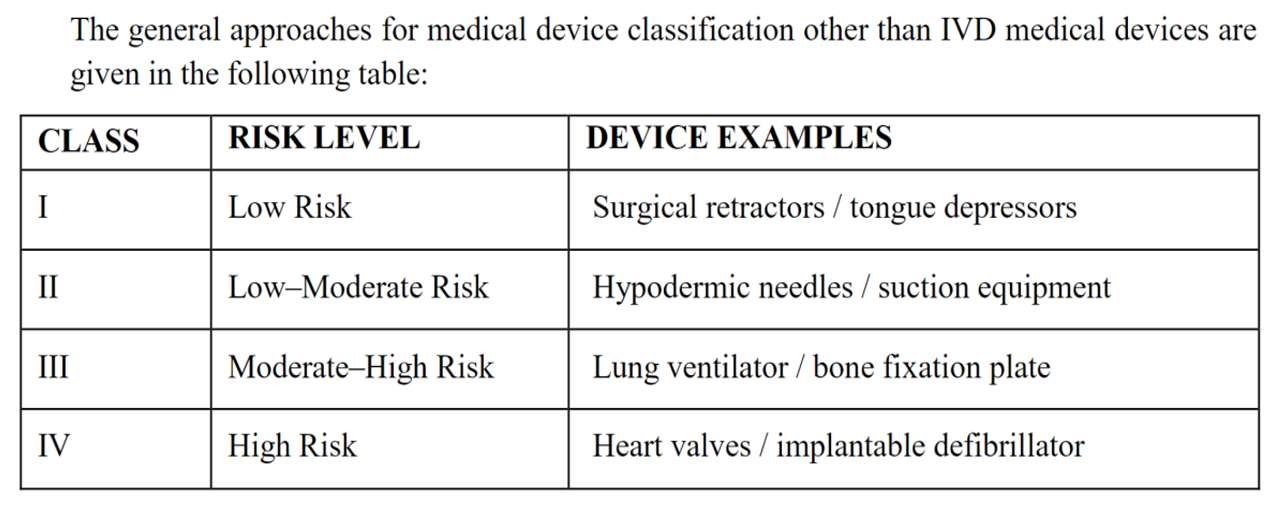
IVD 产品分类:
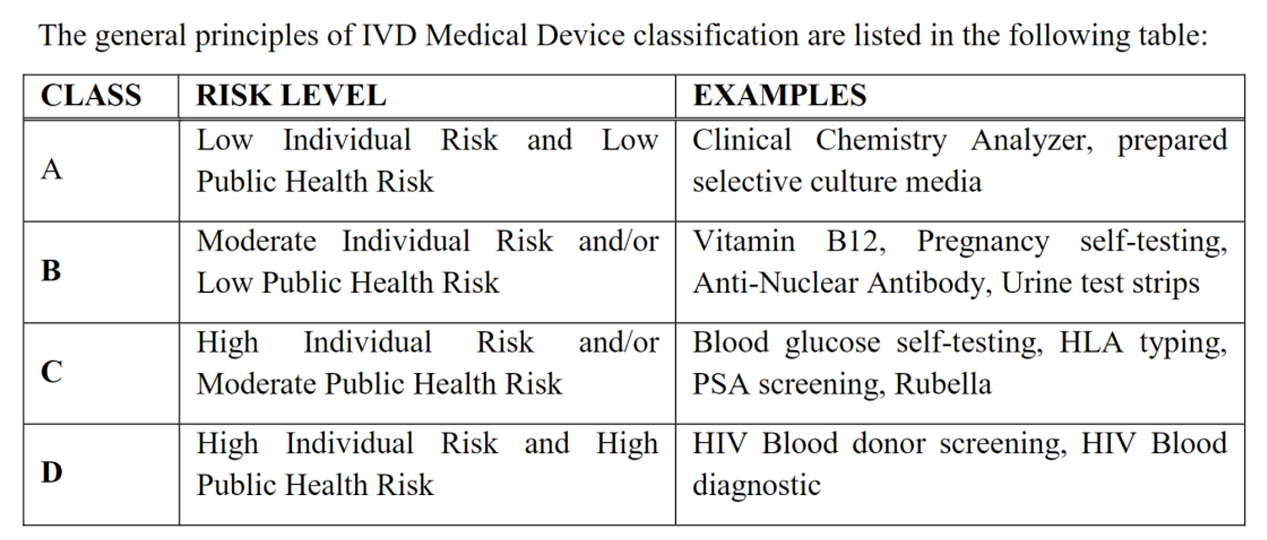
ISO 13485证书
产品信息,包括包装和标签,适用范围涵盖的设备列表,以及相关附加信息
埃塞俄比亚授权代表:授权书和代理协议
自由销售证明或上市许可证明
符合性声明(DOC)
英语
外国制造商应任命一名埃塞俄比亚当地代表,负责代表制造商与监管机构提交申请并与其沟通。
当地代表在进口医疗器械产品时应持有由EFMHACA颁发的进口许可证书。
申请程序必须由当地代表执行。
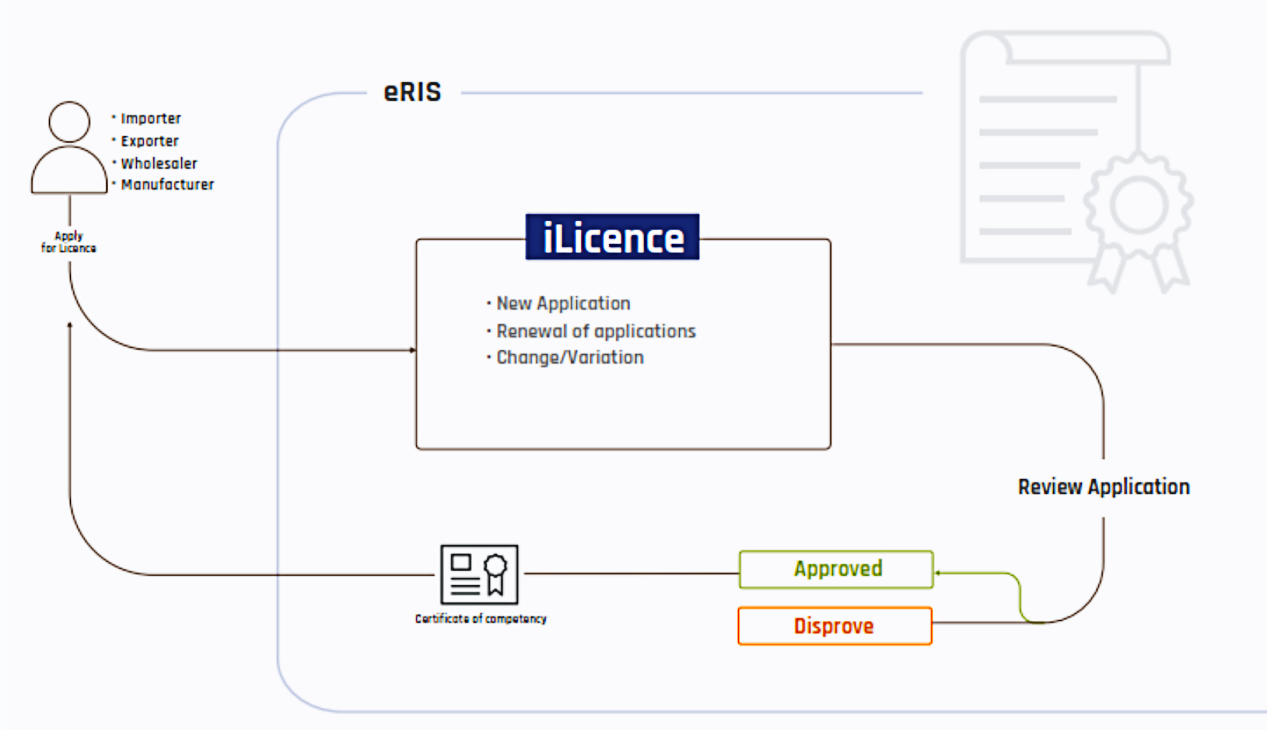
新产品注册:65美元(含文件预审及评估)
新产品注册:65美元(含文件预审及评估)
细微变更:15 美元
主要差异变更:20 美元
年度保留费(续订):30 美元