

哥伦比亚医疗器械监管部门

哥伦比亚监督医疗器械的监管机构为国家药品和食品监督局Instituto Nacional de Vigilancia de Medicamentos y Alimentos(INVIMA)。该机构由哥伦比亚卫生部(MoH)设立,其职责主要包括:法规制定与执行、医疗器械市场准入管理、上市后监督与检查。
Decree No.582/17
MD: Decree No.4725/2005 and its Amendments
IVD: Decree No.3770/2004 and its Amendments
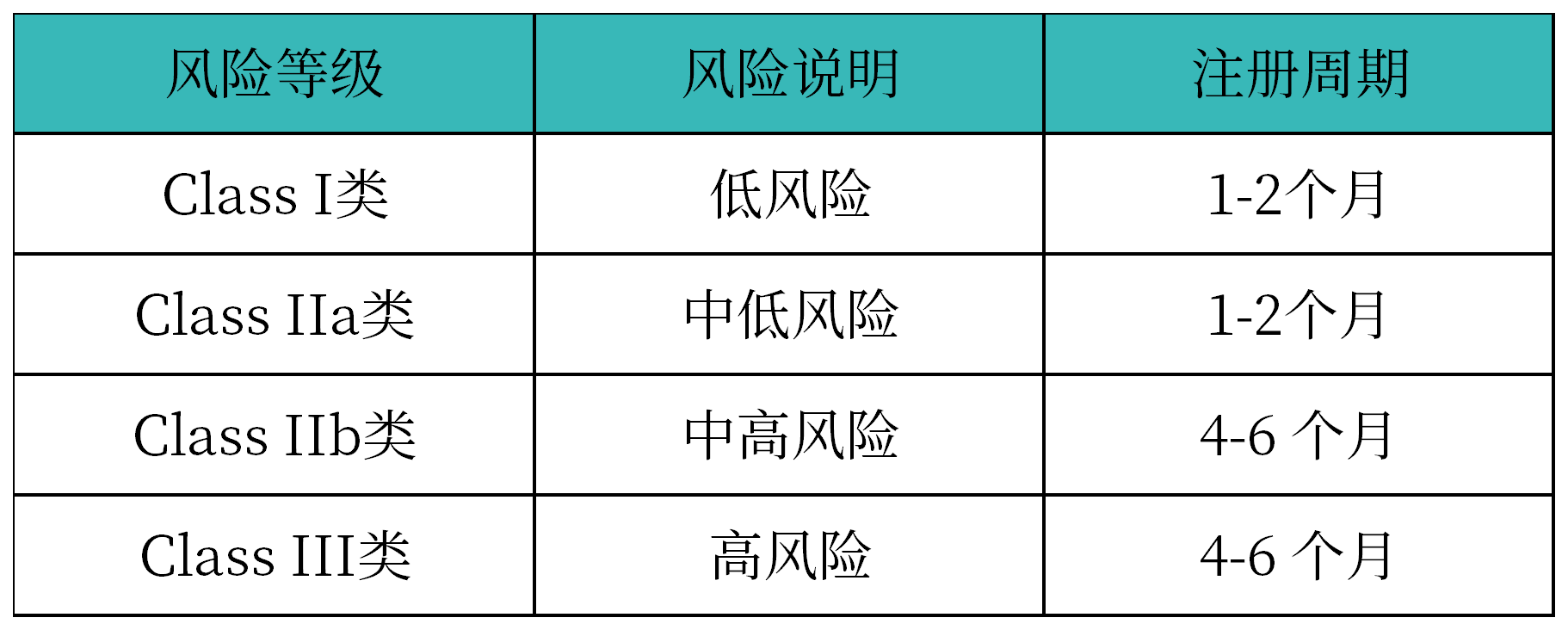
哥伦比亚根据第4725/2005号法令第二章规定,按风险程度和用途将医疗器械分为四个等级:Class Ⅰ(低风险)、Class Ⅱa(中低风险)、Class Ⅱb(中高风险)、Class Ⅲ(高风险)。
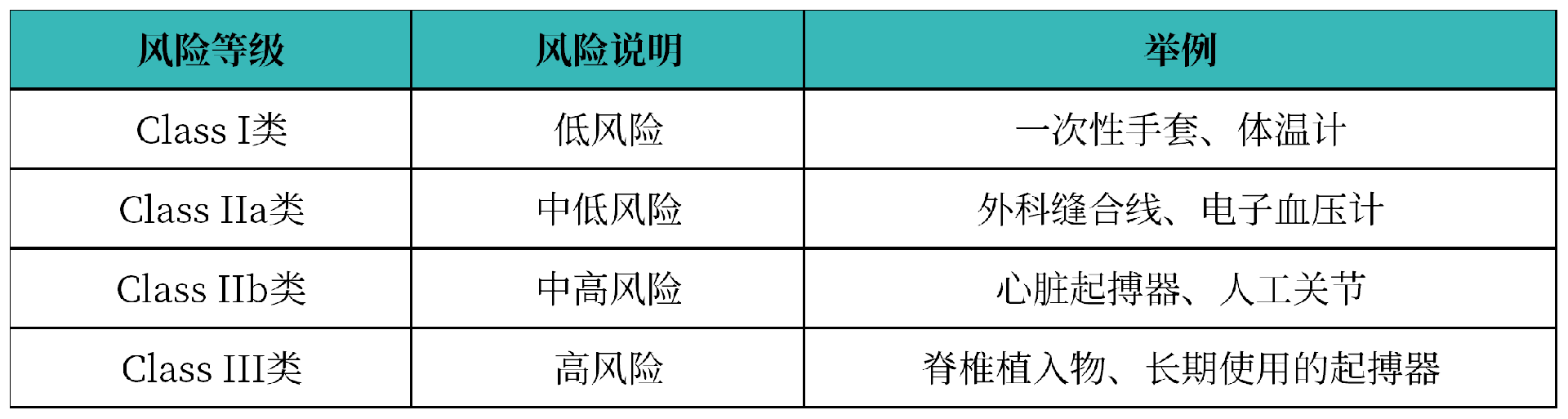
体外诊断试剂(IVD)单独分类,按风险由低到高分为:Class I类、Class II类、Class III类。

① MD和IVD都需要制造商提供ISO13485证书,以证明实际制造设施的质量体系;
② 需委任一名哥伦比亚注册持证人作为当地代表,负责与INVIMA联络;
③ 需提供原产国或澳大利亚、欧洲、加拿大、日本、美国颁发的自由销售证明(FSC),该证明须经海牙认证,且所有文件需翻译为西班牙语。
西班牙语
注:https://www.wiselinkchina.com/static/upload/image/20241212/1733985734143881.png 为纯图片文件,系统无法解析出文本内容,无法展示流程图的具体步骤。
医疗器械:$1011~$1021
体外诊断医疗器械:$700~$1000